Гальваническая коррозия стальных маломерных судов (иногда ошибочно называемая электролизом) может повредить или разрушить подводные металлические части яхт, катеров, лодок и док-оборудования. Когда два разных металла касаются друг друга или электрически соединены проводником и погружены в электролит (электропроводящая жидкость, такая как соленая вода), может произойти электрохимическая реакция. Один из металлов (анод) будет корродировать быстрее, а другой (катод) будет растворяться медленнее.
Что такое гальваническая коррозия?
Гальваническая последовательность морской воды перечисляет металлы в зависимости от их потенциала напряжения и склонности к коррозии. Более активные металлы, быстрее растворяющиеся аноды, находятся в верхней части. Пассивные металлы, катоды, расположены внизу. В вашей яхте может быть коллекция погружных металлических деталей с электрическим соединением, погруженных в соленую воду. Например, нержавеющий опорный вал, потому что он более активен (менее благородный), чем бронзовый винт, начнет растворяться, оставив неповрежденную опору.
Как предотвратить это?

Когда заменить анод?
Эффективность анода зависит от хорошего электрического соединения и прямо пропорциональна его площади поверхности. По мере того, как он корродирует, его площадь поверхности и эффективность уменьшаются. Некоторые производители предлагают заменить аноды, когда они растворились на две трети, но мы рекомендуем заменять их при полуэвентном или частично растворенном. Если аноду позволить полностью растворяться, следующий наименее благородный кусок металла начнет растворяться, и это может быть частью вашей яхты. Помните, что загрязненная вода и высокая температура могут привести к тому, что ваши аноды будут изнашиваться ускоренными темпами, и разумно регулярно проверять их.
Важность крепежных изделий морского типа
Гальваническая коррозия может также произойти в одном изделии, особенно в сплавах, содержащих более одного металла. Взаимодействие между различными металлами в сплаве будет растворять наименее благородный металл, наиболее распространенным примером которого является растворение цинка из многих сплавов цинка / меди (таких как латунь и некоторые бронзы), оставляя слабый, губчатый медный остаток. Вот почему так важно использовать крепежные изделия морского типа (бронза, монель и нержавеющая сталь 316) в подводных приложениях, чтобы они не были разрушены. Чем выше соленость и температура воды, тем больше вероятность коррозии.
Гальванические изоляторы защищают от проблем с питанием

Избавление от кадмия и цинка
Цинк и кадмий - это элементы, используемые в традиционных анодах соленой воды, которые, как предполагается, наносят экологический ущерб. Компоненты сплавов нового поколения анодов не включают кадмий (одно из шести веществ, запрещенных директивой Европейского Союза «Ограничение по опасным веществам») и содержат долю цинка, используемого при изготовлении традиционного цинкового анода (цинк отрицательно влияет на количество кислорода, которое рыба может нести в своей крови). Два компонентаI, алюминий и индий, считаются нетоксичными.
Какой анод подходит именно вам?
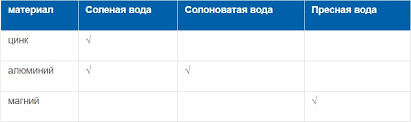
Магний для пресной воды и ТОЛЬКО: поскольку пресная вода гораздо менее проводящая, чем соленая вода, магниевые аноды являются лучшим выбором, потому что они более активны (менее благородны), чем цинк или алюминий, поэтому они более эффективно защищают ваши детали двигателя. Предостережение: не используйте магниевые аноды в любом приложении, отличном от пресной воды, потому что они быстро разъедаются, подвергая вашу лодку и двигатель возможному повреждению.
Алюминий для солоноватой воды: более активный, чем цинк, алюминиевые аноды являются хорошим компромиссом, когда мы говорим о смеси пресной и соленой воды, такой как солоноватая вода дельт реки, или если вы используете свою лодку в различных типах воды. Цинк слишком пассивен для солоноватой воды, где он покрывается пленкой оксида цинка и становится неактивным. Магний корродирует слишком быстро (из-за содержания соли в воде), оставляя вашу лодку без надлежащей защиты.
Все типы анодов для Вашей яхты и катера у нас в каталоге!
